مقدمه بخار :
انرژی به عنوان منبعی با ارزش در طیف وسیعی از صنایع برای هر دو منظور گرمایش و سرمایش استفاده می شود.
انتقال گرما به دو صورت می تواند انجام پذیرد:
۱) مستقیم – که در آن گرما به طور مستقیم از منبع آن به ماده ای که قرار است گرم شود منتقل می شود به عنوان مثال گرم شدن لوله های فلزی با شعله گاز
۲) غیر مستقیم – که در آن انتقال انرژی گرمایی به یک ماده از طریق یک واسط صورت می پذیرد. به عنوان مثال یک کتری که در آن جذب گرما توسط یک اجاق گاز صورت می پذیرد. حرارت از شعله گاز به آب را از طریق پایین کتری و سپس به آب منتقل شده است. در صنعت، بخار برای گرم آب یا روغن حرارتی جهت استفاده در فرایند های مختلف ، تولید می شود .
در صنعت، بخار برای گرم آب یا سایر مایعات فرآیندی جهت کاربردهای صنعتی و تهویه مطبوع از جمله استرلیزه کردن ، رنگ زدایی، گرمایش هوا و تقطیر، تولید می شود.
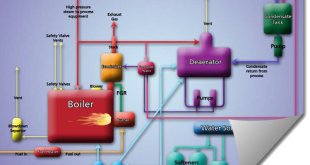
در هر سیستم تولید بخار ابتدا تولید بخار از منبع اصلی آن یعنی دیگ بخار شروع شده و پس از توزیع در سیستم و گرمایش سطوح مختلف ؛ به کندانس تبدیل می شود و دوباره به دیگ بر میگردد .
اصطلاح «آنتالپی » جهت معرفی حرارت و یا محتوای حرارتی استفاده می شود . آنتالپی به طور کلی به عنوان مقدار کل انرژی موجود در یک سیستم تعریف می شود. این مقدار انرژی میتواند به شکل گرما در گازها و یا مایعات یا بخار و یا به صورت انرژی بین پیوند ملکولی باشد به عنوان مثال در سوختها .به طور کلی میتوان گفت آنتالپی مقدار انرژی مورد نیاز جهت برای تغییر حالت فازی یک ماده از مایع به گاز و یا از جامد به مایع می باشد .
بخار چیست ؟
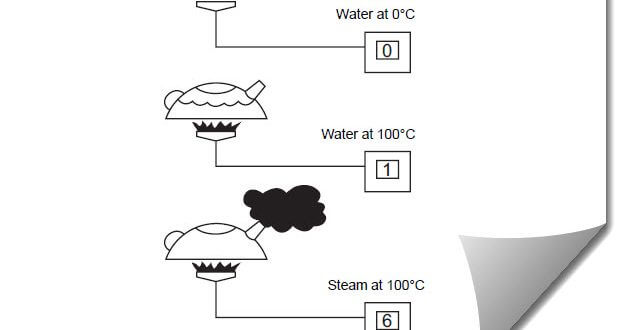
یک کتری قدیمی سوت دار را در آشپزخانه تصور کنید. ما آن را با آب پر کنیم و انرا در معرض گرمای اجاق گاز قرار میدهیم. بعد از چند دقیقه، آب شروع به جوش می کند و بخار از دهانه کتری خارج می شود. دقیقا در کتری پر از آب – معادل یک دیگ بخار – از لحظه شروع حرات دهی تا ظهور بخار چه اتفاقی می افتد ؟
انتقال حرارت از شعله گاز در زیر کتری شروع می شود . با بالا رفتن دما حباب های کوچک بر روی دیوار کتری تشکیل می شوند. پس از مدتی، این حباب ها به سمت بالا رفته و گازهای محلول در آب – که یکی از هوا است – را از آب خارج می کند .
مشاهدات ۱:
حلالیت گازهای موجود در آب با افزایش درجه حرارت آب کاهش می یابد. این پدیده ای است که در هوا زدا (دی اریتور ) استفاده می شود که در مباحث بعدی در خصوص آن توضیح خواهم داد.
حباب های کوچک در پایین کتری گرم می شوند. با گرم شدن کتری این حباب افزایش می یابدو قبل از رسیدن به سطح آب ناپدید می شوند. در حالی که درجه حرارت در پایین کتری به دمای ۱۰۰ºC رسیده است ، در لایه های بالاتر آب ؛ دما کمتر می باشدو پس از بالا رفتن دما لایه های بالایی میتوان شاهد ظهور حباب های بخار بود در همان زمان، روشن است که سطح آب با افزایش درجه حرارت در کتری بالا می رود . این پدیده به طور قابل توجهی از لحظه ای شکل گیری حباب های بخار افزایش می یابد.
مشاهدات ۲:
انبساط آب در زمان گرمایش :
زمانی که مقداری آب را بخار میکنیم ، حجم کل حباب های بخار تولید شده ۱۷۰۰ برابر بزرگتر از حجم آب اولیه می باشد .
در یک زمان مشخص درجه حرارت کتری به ۱۰۰ºC می رسد . در این زمان ؛حبابهای بخار به طور منظم به سطح آب می آیند و فرار کنند. آب شروع به جوش می کند و بخار ظاهر می شود . اگر در این زمان دمای آب و بخار را اندازه گیری کنیم هر دو ۱۰۰ºC خواهد بود .
اگر ما در اینحال گرما دهی را مثلا با زیاد کردن گاز ادامه دهیم ؛ مقدار حباب بخار نیز افزایش خواهد یافت. با این حال، هر چقدر مقدار گرما دهی را تغییر دهیم دمای آب و بخار همان۱۰۰ºC ثابت خواهد ماند .
مشاهدات ۳:
درشرایط جوی( فشار مطلق ۱۰۱۳ میلی بار) آب در دمای ۱۰۰ درجه سانتیگراد می جوشد . آب با درجه حرارت بالاتر از ۱۰۰ درجه سانتی گراد نمی تواند تحت شرایط جوی وجود داشته باشد. بخاری که از آب ۱۰۰ درجه سانتی گراد تشکیل شده است، هم دما با آب می باشد .
اگر به آب جوش حرارت بیشتری داده می شود شروع به تبخیر می کند . علاوه بر حرارت محسوس مورد نیاز برای گرمایش آب ، مقدار قابل توجهی از انرژی (گرمای نهان تبخیر) می بایست جهت تبخیر آب عرضه شود .
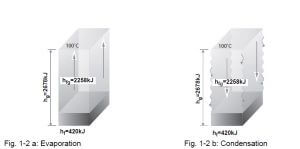
این ((آنتالپی تبخیر )) با نماد hfg نشان داده می شود و مقدار گرمای مورد نیاز برای تبدیل آب ۱۰۰ درجه سانتیگراد به بخار ۱۰۰ درجه سانتی گراد می باشد و hf گرمای مورد نیاز برای رساندن آب ۰ درجه سانتی گراد به آب ۱۰۰ درجه سانتیگراد می باشد بنابراین آنتالپی کل بخار برابر است با مجموع آنتالپی و آنتالپی تبخیر، و توسط نماد hg نشان داده می شود:
hg = hf + hfg
نقطه جوش و تبخیر آب :
شکل زیر نشان دهنده رابطه مصرف گاز جهت جوشاندن و نبخیر آب می باشد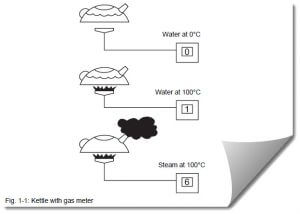
برای شروع آزمایش دبی سنج گاز را روی صفرتنظیم می کنیم . پس از آن دمای آب را به ۱۰۰ درجه سانتیگراد می رسانیم . دبی مصرفی گاز عدد ۱ را نشان می دهد . بیشتر از شش واحد از گاز جهت تبخیر آب مورد نیاز خواهد بود به عبارت دیگر در حدود ۶ برابر انرژی بیشتر جهت تبخیر آب مورد نیاز می باشد .
برای تبخیر آب (رساندن آب از دمای ۱۰۰ºC به بخار ۱۰۰ºC ) در مقایسه با گرم کردن آب (رساندن آب از دمای ۰ºC به آب ۱۰۰ºC ) در حدود ۶ برابر انرژی بیشتر مورد نیار می باشد . این بدان معنی است که ۱ کیلوگرم بخار در دمای ۱۰۰ درجه درحدود شش برابر انرژی حرارتی بیشتری نسبت به اندازه ۱ کیلوگرم از آب در ۱۰۰ درجه سانتی گراد دارد .
اگر حرارت از بخار در دمای ۱۰۰ºC گرفته شود ، کندانس با دمای ۱۰۰ºC تشکیل می شود.
گرمای ویزه آب برابر Kj/KgK ۴٫۲می باشد یعنی برای رساندن دمای آب از ۰ºC به ۱۰۰ºC در حدود Kj 420 = 4.2 × ۱۰۰ انرژی حرارتی مورد نیاز است (hf) و برای رساندن آب از دمای ۱۰۰ºC به بخار ۱۰۰ºC در حدود kJ/kG 2258 انرزی حرارتی مورد نیاز است (hfg ) .این مقادیر در جداول بخار قید شده اند .
مقدار انرژی مورد نیاز برای تبخیر یک کیلوگرم از آب صفر درجه سانتیگراد در شرایط اتمسفریک برابر است با :
hg=hf+hfg=420+2258=2678 Kj
زمانی که گرما بخار به محصول و یا یک مبدل حرارتی منتقل می شود ؛ کندانس تشکیل می شود .گرمای آزاد شده همان گرمای نهان تبخیر hfg خواهد بود و دوباره کندانس ۱۰۰ درجه سانتیگراد تشکیل خواهد شد .
دوستان عزیز در ادامه جهت تکمیل اطلاعات و بررسی جداول بخار به قسمتی از هندبوک ARI ARMATUREN مراجعه و آنرا دانلود نمایید.
دانلودپسورد فایل : utilityprocessdesigner.ir